Категория:Цеолиты — различия между версиями
Kondra s (обсуждение | вклад) |
Kondra s (обсуждение | вклад) |
||
| Строка 2: | Строка 2: | ||
В современной минералогической номенклатуре это большая группа близких по составу и свойствам минералов, в которую входят водные алюмосиликаты (а также бериллосиликаты, цинкосиликаты и бериллофосфаты) кальция и натрия, а также бария, калия и стронция и реже магния и марганца. Цеолиты относятся к подклассу каркасных силикатов. Общую формулу минералов группы цеолитов можно условно выразить как '''A<sub>m</sub>X<sub>p</sub>O<sub>2p</sub>*nH<sub>2</sub>O''', где X = Al, Si. | В современной минералогической номенклатуре это большая группа близких по составу и свойствам минералов, в которую входят водные алюмосиликаты (а также бериллосиликаты, цинкосиликаты и бериллофосфаты) кальция и натрия, а также бария, калия и стронция и реже магния и марганца. Цеолиты относятся к подклассу каркасных силикатов. Общую формулу минералов группы цеолитов можно условно выразить как '''A<sub>m</sub>X<sub>p</sub>O<sub>2p</sub>*nH<sub>2</sub>O''', где X = Al, Si. | ||
| − | + | ==Кристаллическая структура цеолитов== | |
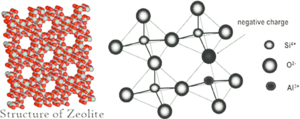
Структура цеолитов характеризуется каркасом из связанных тетраэдров, каждый из которых состоит из четырёх атомов О, окружающих катион. В каркасе позиции тетраэдров нередко могут занимать анионы (OH,F); они заселяют вершину тетраэдра, которая не является общей с соседними тетраэдрами. Эта каркасная структура отличается от других типов тем, что содержит в себе более крупные каналы. Обычно они заселены молекулами H<sub>2</sub>O и внекаркасными катионами, как правило взаимозаменяемыми. В цеолитах очень легко реализуется обмен между катионами, уравновешивающими отрицательный заряд каркаса кристаллической решётки, и катионами в окружающем водном растворе. | Структура цеолитов характеризуется каркасом из связанных тетраэдров, каждый из которых состоит из четырёх атомов О, окружающих катион. В каркасе позиции тетраэдров нередко могут занимать анионы (OH,F); они заселяют вершину тетраэдра, которая не является общей с соседними тетраэдрами. Эта каркасная структура отличается от других типов тем, что содержит в себе более крупные каналы. Обычно они заселены молекулами H<sub>2</sub>O и внекаркасными катионами, как правило взаимозаменяемыми. В цеолитах очень легко реализуется обмен между катионами, уравновешивающими отрицательный заряд каркаса кристаллической решётки, и катионами в окружающем водном растворе. | ||
В гидратированных фазах дегидратация происходит при температурах преимущественно ниже 400°С и в значительной степени обратима: при постепенном нагревании вода может быть полностью удалена без разрушения кристаллической структуры, но при этом вода может быть обратно поглощена в первоначальном количестве либо заменена другими молекулами (аммиаком, сероводородом, этиловым спиртом и т.д.). При этом кристаллическая среда сохраняет однородность и меняются лишь оптические свойства минералов. | В гидратированных фазах дегидратация происходит при температурах преимущественно ниже 400°С и в значительной степени обратима: при постепенном нагревании вода может быть полностью удалена без разрушения кристаллической структуры, но при этом вода может быть обратно поглощена в первоначальном количестве либо заменена другими молекулами (аммиаком, сероводородом, этиловым спиртом и т.д.). При этом кристаллическая среда сохраняет однородность и меняются лишь оптические свойства минералов. | ||
| + | [[Файл:Кристаллическая структура цеолитов.png|мини|Кристаллическая структура цеолитов]] | ||
| + | По сравнению с безводными алюмосиликатами минералы группы цеолитов характеризуются меньшей твёрдостью, меньшим удельным весом, меньшими показателями преломления и более лёгкой разлагаемостью в кислотах. | ||
| + | ==Генезис цеолитов== | ||
| + | При ''эндогенных'' процессах минералы группы цеолитов образуются при низких давлениях на самых последних стадиях низкотемпературных гидротермальных процессов. Как правило, они встречаются в гидротермально изменённых магматических породах, в пузыристых эффузивах (мандельштейнах), особенно в базальтах (при подводных извержениях). Цеолиты встречаются и в пегматитах, где образуются одними из последних либо в пустотах, либо метасоматическим путём за счёт ранее выделившихся минералов. Также цеолиты встречаются в гидротермальных рудных месторождениях и в некоторых современных отложениях горячих источников. | ||
| − | + | При ''экзогенных'' процессах цеолиты образуются в осадочных породах молодого возраста, а также в почвах, в целом характеризуются широким распространением. При образовании цеолитов отмечается последовательность, заключающаяся в том, что сначала выделяются цеолиты, бедные водой и богатые кремнезёмом, а потом — цеолиты, богатые водой и бедные кремнезёмом. | |
| + | ==Области применения цеолитов== | ||
| + | Цеолиты как полезное ископаемое имеют необычайно широкую сферу использования в промышленности и сельском хозяйстве. Они применяются как сорбенты и ионообменники в нефтехимии, как осушитель газов и сред, для очистки питьевых и технических вод, для извлечения радионуклидов, в качестве катализатора, в строительстве, для улучшения почвы, в качестве удобрения, для подкормки животных и т.д. | ||
==Ссылки== | ==Ссылки== | ||
* [https://www.mindat.org/min-4395.html www.mindat.org] | * [https://www.mindat.org/min-4395.html www.mindat.org] | ||
* [https://www.mineralienatlas.de/lexikon/index.php/MineralData?mineral=Zeolite%20group www.mineralienatlas.de] | * [https://www.mineralienatlas.de/lexikon/index.php/MineralData?mineral=Zeolite%20group www.mineralienatlas.de] | ||
| − | + | ==Список литературы== | |
| + | * Сендеров Э.Э., Хитаров Н.И. Цеолиты, их синтез и условия образования в природе // Наука, Москва, 1970 г., 283 стр., УДК: 549.07:549.67. | ||
| + | * Coombs, D. S., Alberti, A., Armbruster, T., Artioli, G., Colella, C., Galli, E., Grice, J. D., Liebau, F., Mandarino, J. A., Minato, H., Nickel, E. H., Passaglia, E., Peacor, D. R., Quartieri, S., Rinaldi, R., Ross, M. I., Sheppard, R. A., Tillmanns, E., Vezzalini, G. (1997) [[Media:Coombs1997.pdf|Recommended nomenclature for zeolite minerals: report of the Subcommittee on Zeolites of the International Mineralogical Association, Commission on New Minerals and Mineral Names]] // The Canadian Mineralogist, 35 (6) 1571-1606 | ||
[[Category:Минералы]] | [[Category:Минералы]] | ||
[[Category:Силикаты]] | [[Category:Силикаты]] | ||
Версия 10:59, 15 мая 2024
Название «Цеолит» введено в 1756 г. шведским минералогом А.Ф. Кронштэдтом (1722 – 1765) как производное от греч. «zeo» – вскипающий (вспучивающийся) при нагревании из-за содержания в минералах значительного количества свободной воды.
В современной минералогической номенклатуре это большая группа близких по составу и свойствам минералов, в которую входят водные алюмосиликаты (а также бериллосиликаты, цинкосиликаты и бериллофосфаты) кальция и натрия, а также бария, калия и стронция и реже магния и марганца. Цеолиты относятся к подклассу каркасных силикатов. Общую формулу минералов группы цеолитов можно условно выразить как AmXpO2p*nH2O, где X = Al, Si.
Содержание
Кристаллическая структура цеолитов
Структура цеолитов характеризуется каркасом из связанных тетраэдров, каждый из которых состоит из четырёх атомов О, окружающих катион. В каркасе позиции тетраэдров нередко могут занимать анионы (OH,F); они заселяют вершину тетраэдра, которая не является общей с соседними тетраэдрами. Эта каркасная структура отличается от других типов тем, что содержит в себе более крупные каналы. Обычно они заселены молекулами H2O и внекаркасными катионами, как правило взаимозаменяемыми. В цеолитах очень легко реализуется обмен между катионами, уравновешивающими отрицательный заряд каркаса кристаллической решётки, и катионами в окружающем водном растворе.
В гидратированных фазах дегидратация происходит при температурах преимущественно ниже 400°С и в значительной степени обратима: при постепенном нагревании вода может быть полностью удалена без разрушения кристаллической структуры, но при этом вода может быть обратно поглощена в первоначальном количестве либо заменена другими молекулами (аммиаком, сероводородом, этиловым спиртом и т.д.). При этом кристаллическая среда сохраняет однородность и меняются лишь оптические свойства минералов.
По сравнению с безводными алюмосиликатами минералы группы цеолитов характеризуются меньшей твёрдостью, меньшим удельным весом, меньшими показателями преломления и более лёгкой разлагаемостью в кислотах.
Генезис цеолитов
При эндогенных процессах минералы группы цеолитов образуются при низких давлениях на самых последних стадиях низкотемпературных гидротермальных процессов. Как правило, они встречаются в гидротермально изменённых магматических породах, в пузыристых эффузивах (мандельштейнах), особенно в базальтах (при подводных извержениях). Цеолиты встречаются и в пегматитах, где образуются одними из последних либо в пустотах, либо метасоматическим путём за счёт ранее выделившихся минералов. Также цеолиты встречаются в гидротермальных рудных месторождениях и в некоторых современных отложениях горячих источников.
При экзогенных процессах цеолиты образуются в осадочных породах молодого возраста, а также в почвах, в целом характеризуются широким распространением. При образовании цеолитов отмечается последовательность, заключающаяся в том, что сначала выделяются цеолиты, бедные водой и богатые кремнезёмом, а потом — цеолиты, богатые водой и бедные кремнезёмом.
Области применения цеолитов
Цеолиты как полезное ископаемое имеют необычайно широкую сферу использования в промышленности и сельском хозяйстве. Они применяются как сорбенты и ионообменники в нефтехимии, как осушитель газов и сред, для очистки питьевых и технических вод, для извлечения радионуклидов, в качестве катализатора, в строительстве, для улучшения почвы, в качестве удобрения, для подкормки животных и т.д.
Ссылки
Список литературы
- Сендеров Э.Э., Хитаров Н.И. Цеолиты, их синтез и условия образования в природе // Наука, Москва, 1970 г., 283 стр., УДК: 549.07:549.67.
- Coombs, D. S., Alberti, A., Armbruster, T., Artioli, G., Colella, C., Galli, E., Grice, J. D., Liebau, F., Mandarino, J. A., Minato, H., Nickel, E. H., Passaglia, E., Peacor, D. R., Quartieri, S., Rinaldi, R., Ross, M. I., Sheppard, R. A., Tillmanns, E., Vezzalini, G. (1997) Recommended nomenclature for zeolite minerals: report of the Subcommittee on Zeolites of the International Mineralogical Association, Commission on New Minerals and Mineral Names // The Canadian Mineralogist, 35 (6) 1571-1606
Подкатегории
В этой категории отображается 17 подкатегорий из имеющихся 17.
П
- Подгруппа брюстерита
- Подгруппа гарронита
- Подгруппа гейландита
- Подгруппа гмелинита
- Подгруппа дакиардита
- Подгруппа жисмондина
- Подгруппа клиноптилолита
- Подгруппа маццита
- Подгруппа натролита
- Подгруппа паулингита
- Подгруппа стильбита
- Подгруппа томсонита
- Подгруппа феррьерита
- Подгруппа филлипсита
- Подгруппа фоязита
- Подгруппа шабазита-левина
- Подгруппа эрионита
Страницы в категории «Цеолиты»
Показана 51 страница из 51, находящейся в данной категории.